一般毒理学研究
具备开展化学药物、中药、生物技术药物临床前安全性评价的能力,尤其是针对新型疫苗、基因治疗产品、新型抗体、蛋白多肽、细胞治疗产品等创新生物技术药物国内率先建立了全面的安全评价技术体系,具有丰富的产品评价经验和技术优势。
可承接啮齿类(大鼠、小鼠)、非啮齿类(家兔、豚鼠、犬、猴)及特殊模型动物的一般毒性试验研究。
具体如下:
• 毒性剂量探索验
• 急性毒性试验
• 亚慢性毒性试验
• 长期毒性试验
• 致癌性试验
• 制剂安全性试验(溶血、刺激、过敏)
• 免疫原性试验
• 免疫毒性试验
• 光毒性、光过敏试验
• 生物分布研究(实时定量PCR、活体成像、免疫组化等)









发育和生殖毒理学(DART)研究
作为国内首家开展GLP条件下发育和生殖毒性研究的实验室,具有研究经验丰富的专业团队,能够开展化药、中药、疫苗等生殖发育全套毒性试验。可承接服务的动物种属包括大鼠、小鼠、家兔。
可提供研究服务如下:
• 生育力和早期胚胎发育毒性试验(I段试验)
• 胚胎-胎仔发育毒性试验(Ⅱ段试验)
• 围产期发育毒性和母体功能试验(Ⅲ段试验)
• 多代繁殖试验
• 儿科用药安全性评价的幼年动物试验
• 母体及仔的毒代动力学研究
• 毒性筛选试验(体外全胚胎培养模型、体外卵巢颗粒细胞模型、3D卵泡体外培养模型等)

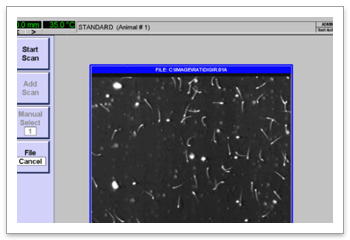
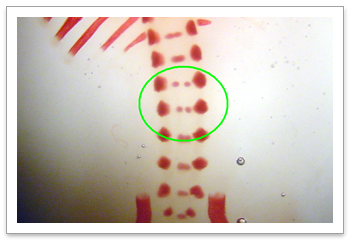

遗传毒理学研究
中心是国内首批在GLP条件下开展遗传毒性实验的实验室,拥有独立的Ames实验室和细胞培养室,以及全自动细胞计数仪、显微成像系统等先进的体外研究设备。专业技术人员经验丰富,确保提供高品质的药物潜在致突变性、致癌性研究服务。我们已积累大量历史背景数据,可提供遵从GLP管理规范,并符合NMPA,US FDA和OECD指导原则要求的ICH标准组合全套遗传毒性研究。
建立肝细胞彗星电泳、外周血红细胞微核实验、体内Pig-A基因突变检测等体内遗传毒性多终点检测方法;
建立Bhas42细胞致癌性检测新方法、转基因C57-ras致癌小鼠模型等开展短期致癌性预测模型的研究。
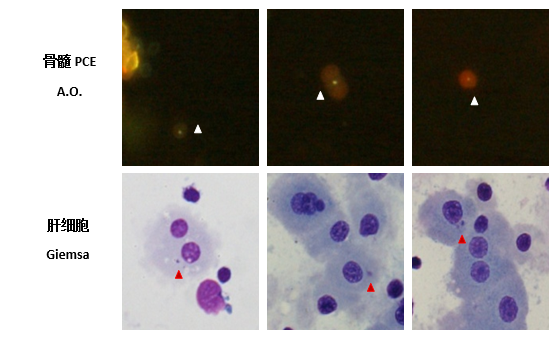
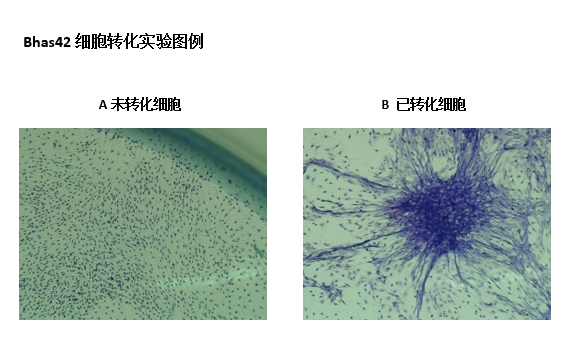

安全药理学研究
中心拥有清醒犬心血管、呼吸遥测系统、自发活动监测系统、啮齿类呼吸测定系统、全自动膜片钳系统、高内涵细胞成像仪、实时细胞功能分析仪等先进仪器设备,可以提供遵循新药临床前安全评价国际规范ICH(S7A,S7B)、CFDA技术指导原则的安全药理学研究服务。可承接服务的动物种属包括大鼠、小鼠、犬、猴。
可提供研究服务如下:
• 中枢神经系统安全性评价(功能观测组合实验/改良的Irwin's实验)
• 心血管系统安全性评价(心电图、血压、心率、清醒动物体温、活动度)
• 呼吸系统安全性评价(啮齿类及非啮齿类动物的呼吸频率、潮气量、每分钟通气量等)
• 心血管功能体外评价体系(离子通道、心肌搏动检测等)
• 肠胃系统安全性评价
• 泌尿系统安全性评价


受试物分析、生物分析、药代毒代研究
中心是国内最早开展符合GLP规范的生物大分子药物药代毒代动力学研究的实验室,具有丰富的研究经验;具备开展创新生物技术药和小分子化学药的药代、毒代研究,可同时满足FDA、EMA和中国药典对生物分析的要求。
可提供研究服务如下:
• 各类受试物的配制
• 符合GLP规范的受试物制剂分析(包括制剂配制方法研究、分析方法建立与验证、制剂的浓度、均一性、稳定性的分析测定)
• 化学药物和生物大分子药物生物分析方法开发和验证(液相色谱-串联质谱法,配体结合测定法)
• 化学药物和生物大分子药物的药代毒代研究与生物分析数据的分析处理。
• In Vitro ADME,模型预测







临床检验与病理学检查
中心是国内首家通过美国CAP认证的GLP临检实验室,2015年临床检验实验室通过了CNAS认可,成为合格的能力验证提供者并每年组织全国GLP机构临床生化能力验证工作。
可完成符合GLP规范的啮齿类和非啮齿类动物的大体解剖、石蜡及冰冻切片制片、HE染色及特殊染色,电镜标本的制备,免疫组化和免疫荧光、原位杂交等工作。可提供符合GLP规范的急毒试验、长毒试验、刺激性试验及致癌性试验及生殖毒性试验的组织病理评价及报告,提供单克隆抗体及基于抗体药物的组织交叉反应研究和报告,并进行符合OECD规范要求的病理同行评议。






